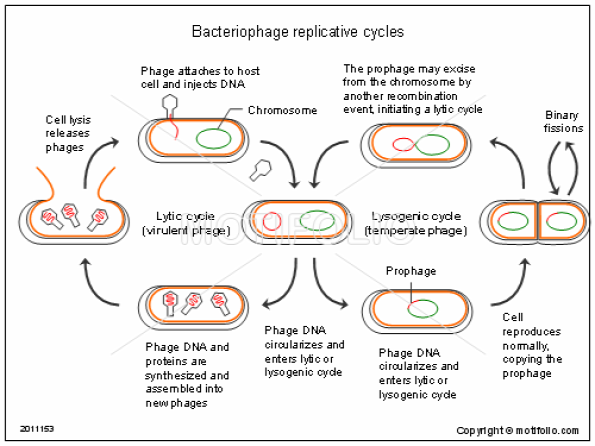
Sikeres génterápiát alkalmaztak az örökletes izombénulás ellen, a Pentagon és az FBI szakértői a módszer alapjait jelentő technika veszélyességét mérlegelték, ugyanez a technika alkalmas lehet a malária felszámolására olyan módon, hogy génmódosított maláriaszúnyogok, amikben a malária nem él túl, idővel kiszoríthatják azokat a szúnyogpopulációkat, amik a maláriát terjesztik. Ugyanennek a CRISPR-Cas9-technikának alkalmazása lehetővé teszi, hogy még a megtermékenyülés előtt meggátolják egy örökletes betegség kialakulását ős-hímivarsejtek génállományának módosításával.
Miről is van szó?
Múlt hét szerdán vált hivatalossá a hír, miszerint a Torontóban sikerrel alkalmaztak génterápiát egy 14 éves betegnél egy biztos bénulással járó örökletes betegség, a Duchenne-féle izomdisztrófia megfékezésére. Egyre közelebb kerül a tudomány ahhoz, hogy most még halálos kimenetelű vagy az életminőséget súlyosan rontó betegségek még a mostani betegek életében gyógyíthatóvá váljanak. A Duchenne-féle izomdisztrófia genetikai oka, hogy a disztrofin génjét kódoló DNS-szakasz hibája. A fehérje elengedhetetlenül fontos a normális izomműködésekhez, több más struktúrfehérjével együtt kapcsolódva teszi lehetővé az izommozgások molekuláris élettani alapját.
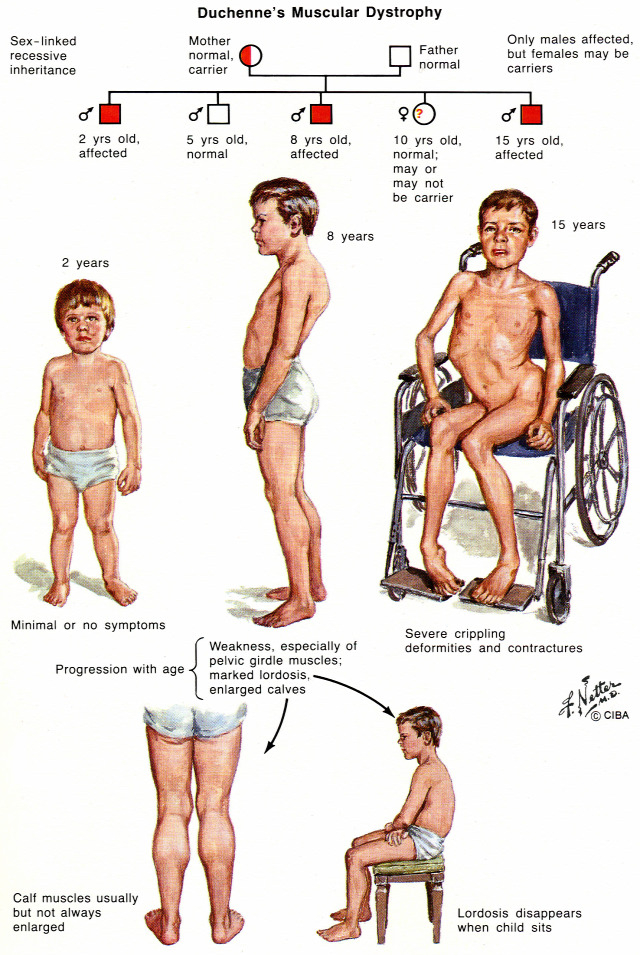
Abban az esetben, ha valami miatt a disztrofin génje több példányban vagy egy ritkább változatban van jelen, kialakul a Duchenne-disztrófia, ami az életkor előrehaladtával folyamatos bénuláshoz vezet több olyan folyamaton keresztül, amik az izomsejtek elhalásához vezetnek. Például az izomsejtek nem tudják kontrollálni, hogy mennyi káliumiont engedjenek be. A beteg egyre gyengébb lesz, végül teljes ellátásra szorul, a betegség utolsó stádiumában pedig már a légzőizmok is működésképtelenné válhatnak, így a beteget lélegeztetőgéppel kell lélegeztetni. Nem véletlen tehát, hogy a rettegett izomsorvadás ennyire az érdeklődés középpontjában van.
Az American Journal of Human Geneticsben januárban fog megjelenni nyomtatásban is az a cikk, amiben Daria Wojtal és Dwi Kemaladewi munkatársaival arról számolnak be, hogy hogyan alkalalmazták a génterápia egyik legígéretesebb módját a betegség gyógyításában. Sikerült elérniük többek közt azt, hogy a disztrofin-gén fölösleges példányai az érintett sejtekben és azok őssejtjeiben eltűnjenek. Mindezt pedig egy víruson keresztül bevitt mesterséges gén bevitelével sikerült megvalósítaniuk. A génterápiához úgynevezett lentivirális vektort alkalmaztak, azaz a retrovírusok egy altípusába tartozó lentivírus fertőzőképességéért felelős génjeit eltávolították, helyére a molekuláris javítást lehetővé tevő gént szerkesztették, majd ezt juttatták be sikeresen a beteg sejtjeibe, ahol a vírus, ha úgy tetszik, a javított génekkel fertőzte meg a célsejteket.
Ugyanezzel az eljárással gyorsabban fejleszthetők biológiai fegyverek is
Néhány héttel ezelőtt az USA-ban a Pentagon és az FBI szakértői tanácskoztak azzal kapcsolatban, hogy a CRISPR-Cas9-technika alkalmazásával létrehozott génmódosított élőlények milyen ökológiai kockázatot jelenthetnek, másrészt mekkora a valószínűsége, hogy terroristák esetleg minden korábbinál patogénebb kórokozókat állítsanak elő biológiai fegyverként való alkalmazás céljából. Természetesen a génmódosított élőlényekkel kapcsolatos kockázatok korábbról is ismertek voltak, a mostani technika azért kapott kitüntetett figyelmet, mert relatív egyszerűbb és olcsóbb, mint az ezt megelőzőek.
Sokmillió életet is menthet
Szintén viszonylag új, hogy olyan maláriaszúnyogokat hoznának létre a gene drive technikával, amikben nem él túl a szúnyog által hordozott malária kórokozója, ilyen módon a genetikailag módosított szúnyogpopuláció kiszoríthatja az eredeti, maláriát terjesztő populációkat, felszámolva ezzel a malária terjedését szerte a világon. Hasonlóan, a ,ódszer kihasználásával lehetne a maláriaszúnyog-populációt részlegesen ivarképtelenné tenni.
És a "szuperszúnyogok"?
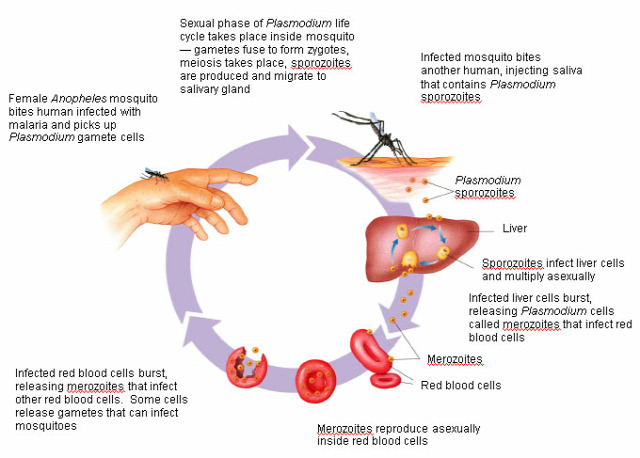
Az előbb említett washingtoni konferencián biztonsági szakértők nem tartották valószínűnek azt a bulvár által felkapott hírt, ami szerint a terroristák szuper-moszkítókat hoznának létre. Viszont nem zárható ki, hogy az új módszerrel genetikailag módosított élőlények jelentsenek kockázatot többek közt azáltal, hogy kiszoríthatják a természetben előforduló fajtársaikat.
Betegségek megelőzése, a magzati kor előtt?
Szintén nemrég egy konferencián olyan, eddig még csak egéren alkalmazott technika alkalmazását vetették fel kutatók, amiben átszabott ős-ivarsejtekből létrejövő hímivarsejtekkel végezhető mesterséges megtermékenyítést valamilyen örökletes betegség kialakulásának megelőzésére. Tehát elvben gyógyíthatóak lennének betegségek, még a megtermékenyülés előtt.
Mi képzi mindezek alapját?
Normális esetben, ha a egy élő sejtben a DNS egy szakasza károsodik, a károsodás a sejt belső hibajavító rendszere felismeri, a sérült szakaszt kivágja és a helyére visszaépíti az eredetit, természetesen mindezt számos köztes lépésben.
A folyamatban viszont van olyan pont, aminél kis trükkel el tudják érni a kutatók, hogy ne az eredeti gént vagy géneket jelentő szakasz épüljön vissza be, integrálódjon a sejtmag DNS-ébe, hanem bizonyos megkötések közt szinte bármi más. Az ilyen módon módosított DNS természetesen a sejt osztódást követő utódsejtjeiben is jelen lesz, valamint már nem osztódó testi sejtek esetén a sejt működése a beavatkozástól függő módon változik meg.
Képek: pinimg.com, millerandlevine.com


 Sophos Naked Security
Sophos Naked Security Securelist
Securelist cyber-secret futurist
cyber-secret futurist I'm, the bookworm
I'm, the bookworm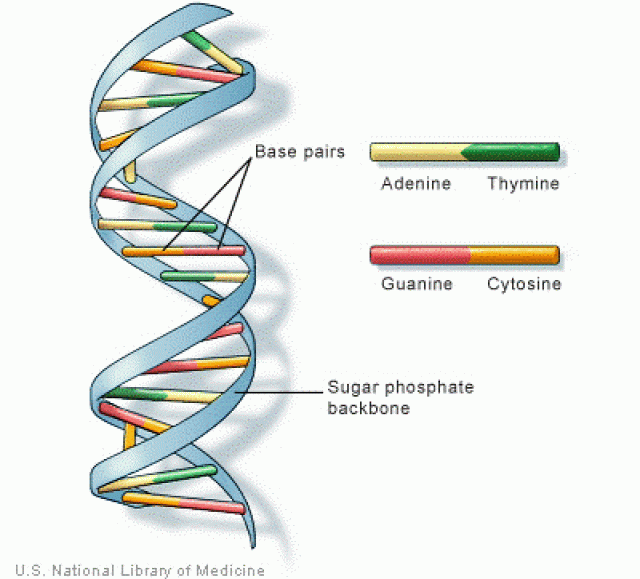
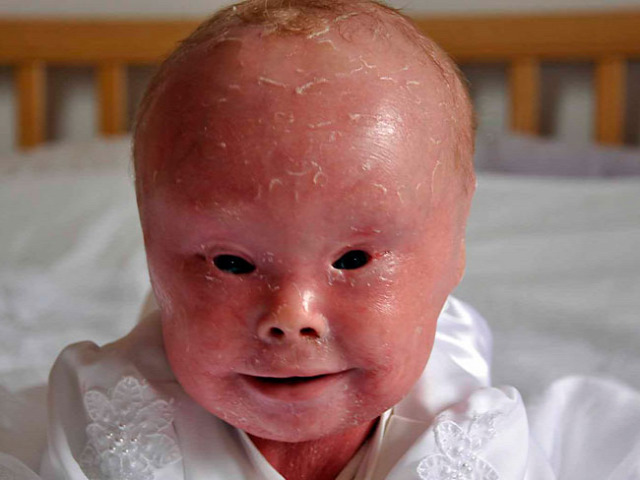
 Augusztusban eléggé erős videót töltöttek fel a 14 éves fiúról, aki egy meglehetősen ritka örökletes betegséggel született, ami miatt a bőre annyira sérülékeny, hogy gyakorlatilag folyamatosan kötözni kell, hogy a helyén maradjon.
Augusztusban eléggé erős videót töltöttek fel a 14 éves fiúról, aki egy meglehetősen ritka örökletes betegséggel született, ami miatt a bőre annyira sérülékeny, hogy gyakorlatilag folyamatosan kötözni kell, hogy a helyén maradjon.